Заход 2. Про то как сворачивать свернутое и гамать в игры науки ради.Третичная структура белков - это пространственная трехмерная структура, образующаяся в результате взаимодействий радикалов. Как это происходит уже должно быть понятно из прошлой части.
Напомню: гидрофобные радикалы аминокислот будут преимущественно собираться внутри благодаря гидрофобным взаимодействиям, образуя более плотные структуры; гидрофильные ионизированные и неионизированные полярные – по большей части окажутся на поверхности глобулы (и определят его растворимость в воде, кстати). Некоторые из них все же окажутся внутри глобулы, где будут взаимодействовать друг с другом, образуя ионные или водородные связи. Схематично связи, образующие третичную структуру белка, можно увидеть на рисунке 6.
Все (или большинство) указанных связей довольно слабые и могут легко разрушаться при тепловом взаимодействии, воздействии сильных кислот или оснований, полярных растворителей (вспомним про спирт «денатурат») и радиации, конечно. Происходит распад третичной структуры, денатурация белка. И его свойства меняются, но его первичная аминокислотная структура – нет. Все этот процесс видели много раз, при жарке яичницы, например. Но в клетке изменение нативной структуры для белка очень нежелательна, он теряет свою функцию.
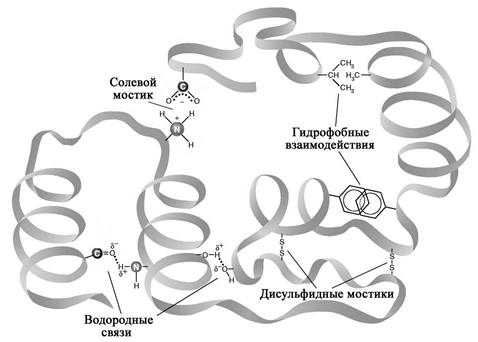 рис. 6
рис. 6Белки способны и к небольшим изменениям конформации, т.е. обладают т.н. лабильностью. Это происходит все по той же причине слабых связей (но их множество!), поддерживающих третичную структуру. Просто одни связи рвутся, а другие – образуются. И таким образом, кстати, регулируется работа ферментов в живой клетке, что отображено на рис. 7, где небелковый активатор меняет структуру молекулы. Но более подробно вдаваться в это не будем, а вернемся к собственно белковой структуре.
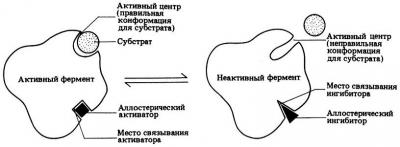 рис. 7
рис. 7Четвертичная структура – это тоже пространственная структура белка, но образованная соединением нескольких полипептидных цепей. Такие белки называют олигомерными, а входящие в них цепи – протомерами. Примером может быть всем известный гемоглобин.
Как теперь понятно, первичная структура (т.е. последовательность аминокислот в цепи) определяет вторичную структуру, та в свою очередь определяет третичную, ну и обе они – четвертичную. Более того, активный центр белка состоит из аминокислот, находящихся не рядом на полипептидной цепи, но оказывающихся рядом после сворачивания ее в нативную форму, сродство к субстрату так же определяется формой молекулы. Т.е. структурой определяется и форма, и функция. А структура зиждется на первичной последовательности и свойствах самих аминокислот.
И тут, казалось бы, все замечательно: пептидная цепь сворачивается в нужную структуру в процессе с красивым названием фолдинг, и мы получаем работающий белок. Но не тут-то было, потому что возникают некоторые проблемы.
Первая проблема заключается в том, что полипептидную цепь можно свернуть очень многими способами, она длинная. Белковые молекулы обычно имеют массу в десятки и сотни килодальтонов, бывают и больше (обозначают «кДа» - дальтоны это то, что в школе называли «молекулярная масса»). А это последовательности из сотен и тысяч аминокислот! Для цепи из 100 остатков число возможных конформаций ~10
100. Но в клетке белки сворачиваются именно так, как нужно (за редкими паталогиями)! И довольно-таки быстро, а ведь процесс сворачивания простым перебором вариантов занял бы ~ 10
80 лет. Этот феномен назван
«парадокс Левинталя» (и цифры взяты из этой статьи в Википедии, кстати).
В настоящее время считается, что сворачивание в нативную структуру происходит так, чтоб молекула имела минимальную свободную энергию (привет от химической термодинамики и самоубывающей энтропии!). Это говорит о том, что по первичной последовательности можно предсказать форму и функцию белка. И это хорошо, потому что нам это крайне необходимо уметь делать, иначе и расшифровка геномов мало что дает, кроме последовательности «букв». А хотелось бы понимать, что это за последовательность и как работает кодируемый ей белок. Но мы все равно практически не умеем это предсказывать, и это крайне плохо.
За подробностями столь печальной ситуации отсылаю к хорошей статье
«Проблема фолдинга белка», за которую надо поблагодарить отчасти и нашего форумчанина. (Ладно, тут без дифирамб, споем в другой теме и потом: я еще не прочитал вторую повесть к своему стыду.)
А мы отметим, что решение этой "проблемы фолдинга" требует больших компьютерных мощностей. И тут все мы можем помочь благому делу. Дело в том, что существует сеть распределенных вычислений для решения задачи по определению структуры белков. А у нас у всех есть компьютеры, которые частенько простаивают. И надо всего лишь присоединиться к этой сети, скачав себе
скринсейвер Rosetta@home. (Я вот раньше помогал SETI, но инопланетяне что-то не торопятся. А вот ВИЧ, рак и болезнь Альцгеймера уже здесь – поэтому лучше все-таки заняться белками, ничего при этом не делая. Последуйте моему примеру.)
Еще один интересный момент в задаче по предсказанию третичной структуры белка заключается в том, что человеческий мозг с ней справляется лучше компьютера. И была создана
игра-головоломка под названием «Fold it» («Сверни это»). Каждый может сам попробовать посворачивать белки в нативную форму. Русский интерфейс присутствует.
(Тут и конец этой маленькой и единственной рекламной паузе) 
.
Второй проблемой оказывается то, что в клетке довольно тесно. Другие молекулы могут банально помешать правильно свернуться полипептидной цепи в белок. Да и ползущая при трансляции из рибосомы цепь полипептида начинает сворачиваться уже при длине в несколько десятков аминокислотных оснований. И это не очень хорошо, ведь свернуть-то надо оптимальным образом всю цепь, а не начальный участок.
И вот у нас имеется ситуация, когда в процессе фолдинга белка требуются помощники. Или наоборот – надо помешать сворачиванию, например, для того чтоб протащить цепочку полипептида через мембрану. А так как "спасение утопающих – дело рук самих утопающих", то этим занимаются тоже белки, имеющие собирательное название «шапероны»
2.
Про них дальше речь и пойдет.
________________
2 Шаперон (от англ. chaperone)— одно из названий наставника и помощника молодого человека или девушки, когда последним требуется поддержка со стороны взрослого опытного человека, в частности, обладающего большими юридическими правами. Термин используется преимущественно во Франции и Великобритании.



